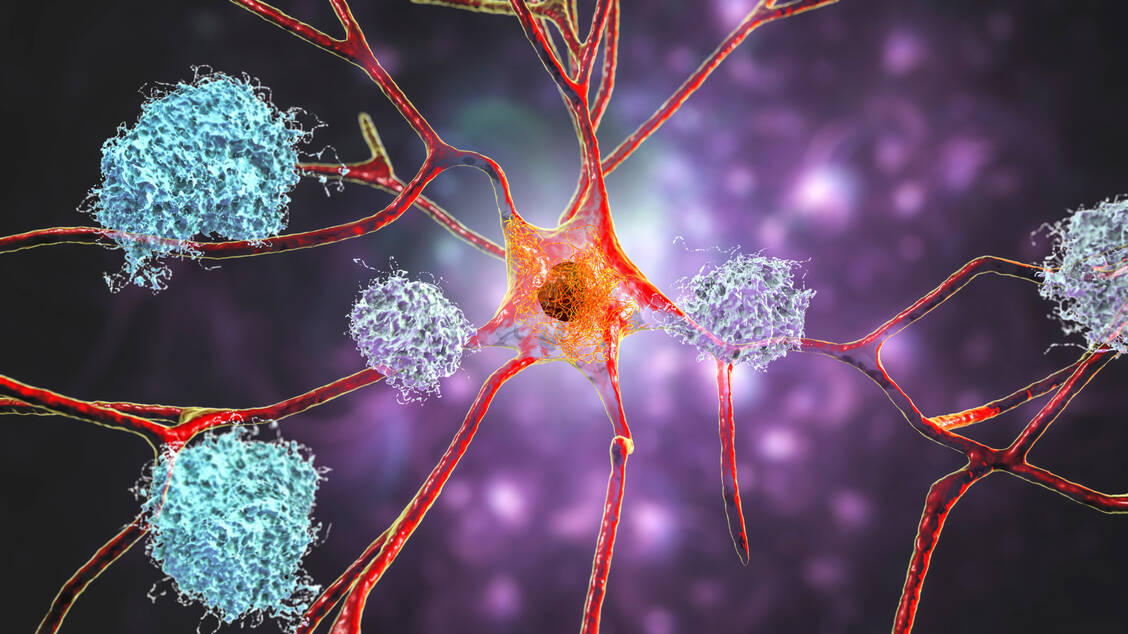
Tau-Proteine sind im Zytosol einer Zelle lokalisiert und binden an Mikrotubuli. Manche neurodegenerativen Erkrankungen sind dadurch gekennzeichnet, dass sich fehlerhafte Tau-Proteine in Zellen zu Aggregaten zusammenlagern. Zu diesen Tauopathien gehören zum Beispiel die Alzheimer- und die Parkinson-Krankheit.
Prionen sind Erreger übertragbarer schwammartiger (spongiformer) Enzephalopathien (Gehirnschädigungen) wie der Creutzfeld-Jakob-Krankheit. Es handelt sich nicht um Bakterien, Viren oder Pilze, sondern um fehlgefaltete, pathologisch zusammengelagerte Prion-Proteine.